Im Juni vergangenen Jahres setzte die Firma Philips eine Sicherheitswarnung für eine Reihe von Beatmungsgeräten ab. In ihnen löst sich ein Dämmschaum auf. Feine Teilchen davon können in die Lunge gelangen. Im August 2021 beginnt die US-Food and Drug Administration (FDA) am Firmensitz von Philips Respironics Inc. in Murrysville bei Pittsburgh zu ermitteln. Die Ergebnisse der Untersuchung sind niederschmetternd. Das Problem war dort nämlich schon länger bekannt. In Österreich sind geschätzte 35.000 Personen von dem gravierenden Mangel betroffen. Ein Mangel, der schwere gesundheitliche Schäden bewirken könnte. Und was passiert von Amts wegen? Am 29. Juni 2021 versteckt das zuständige Bundesamt für die Sicherheit im Gesundheitswesen (BASG) eine Sicherheitswarnung auf seiner Homepage. Menüpunkt: Markbeobachtung, Unterpunkt: amtliche Nachrichten, dort derzeit auf Seite acht. Eine Information der Öffentlichkeit bleibt aus. Außer sich auf europäischer Ebene abzusprechen, unternehmen sie nichts. Die Betroffenen können nur hoffen, dass sie auf vernünftigen ärztlichen Rat zurückgreifen können.
Das Schutzniveau in Österreich liegt low
Wer ist dieses Bundesamt für die Sicherheit im Gesundheitswesen, das im Schadensfall bei Medizinprodukten zuständig ist? Bereits der Gesetzestext lässt erkennen, dass diese Behörde nicht wirklich einschreiten soll. Im entsprechenden Errichtungsgesetz heißt es bei den Zielbestimmungen im Paragrafen eins nämlich:
Zur Wahrung der Wirksamkeit, Sicherheit und Qualität von Arzneimitteln, Gewebe und Medizinprodukten sowie zur Bekämpfung übertragbarer und nicht übertragbarer Krankheiten ist ein hohes Niveau des Gesundheitsschutzes unter Beachtung des Standes der Wissenschaften anzustreben.
… ist ein hohes Niveau … anzustreben. So formuliert kein Gesetzgeber, der scharfe Kontrollen und vorausschauendes Einschreiten bei der Kontrolle von Medizingeräten wünscht. Außerdem ist das Amt zur Unparteilichkeit verpflichtet. Das steht im Paragrafen neun des entsprechenden Gesetzes. Was im Ergebnis der internen Rechtsauslegung dazu führt, die wirtschaftlichen Interessen der Firmen höher anzusetzen als die Gesundheit der Anwender*innen.
Ein Beispiel.
Dämmmasse aus Beatmungsgeräten gelangt direkt in die Lunge
Wie sehen diese „Probleme“ (so das BASG in seiner Sicherheitsmitteilung) im Zusammenhang mit dem schalldämpfenden Schaumstoff in den Philips-Geräten konkret aus? Semiosis liegen Fotos eines entsprechenden Gerätes vor. Die Philips BiPAP S/T-One Serie Auto SV hat ein Techniker im Wiener AKH demontiert. Wenn Menschen unter kurzzeitigen Atemstillständen im Schlaf leiden (Schlafapnoe), kommt das Gerät in der Nacht im Dauerbetrieb zum Einsatz.


Wir erkennen schwarze Schaumstoffmasse, die sich auflöst und abbröckelt. Sie besteht aus Polyester-basiertem Polyurethan und war in einem Gerät der Firma Philips verbaut. Der Dämmschaum kann sich in „bestimmte Partikel“ zersetzen, wie die Firma Philips in ihrer Sicherheitsmitteilung schreibt, die dann
in den Luftweg des Gerätes gelangen und vom Benutzer aufgenommen und eingeatmet werden können.

FDA: Acht schwere Versäumnisse bei Philips
Die FDA hat den Fall vor Ort eingehend untersucht. Dabei hat sie acht Beobachtungen, „observations“, notiert. In jedem dieser Beobachtungen werden Versäumnisse des Herstellers aufgeführt. Die wichtigsten behandeln die inadäquate Risikoanalyse im Haus. Außerdem war die Firma nicht-ausreichende präventiv und korrigierend tätig. Besonders gravierend fällt dabei die Beobachtung ins Gewicht, dass Philips aufgrund firmeninterner Tests und Überprüfungen schon jahrelang hätte wissen müssen, dass der betreffende Schaumstoff problematisch sein könnte.

Zitat aus dem FDA-Bericht: Specifically, there were at least fourteen instances, assessments, and/or test reports, dated from 04/01/2016 to 01/22/2021, where your firm was aware of issues and concerns related to potential foam degradation and/or Volatile Organic Compound (VOC) emissions with various Sleep and Respiratory care devices (…)
Typischerweise erfolgt auf diese Ermittlungen ein Warnbrief der US-Behörde. Bislang ist der laut öffentlich einsehbarer Datenbank aber nicht versendet worden. Jedenfalls ist die FDA der Ursache der Produktwarnung auf den Grund gegangen.
In Österreich wird getauscht
In Österreich werden die Beatmungsgeräte ausgetauscht. Philips hat eingeschriebene Briefe an die Betroffenen versendet, heißt es. Wie viele diese wirklich erhalten haben, ist unbekannt. Wie viele Geräte bisher ausgetauscht wurden, ebenso. Da sie im Rahmen einer medizinischen Therapie eingesetzt werden, ist dieser Prozess besonders haklich.
Für mindestens eine Person kommt das zu spät
Für mindestens einen Patienten kommt das alles zu spät. Die Ärzte haben in seiner Lunge bereits Veränderungen festgestellt, die mit dem Einatmen der Partikel des Schaums erklärbar sind. Die Fotos oben stammen aus dem Gerät, das dieser Patient verwendet hat.
Die Histologie ergab wieder entzündliche Veränderungen und zwar genau solche, wie sie seit vielen
Jahren bei Belastung durch Schaumstoff-Partikel bekannt sind.
So heißt es in der entsprechenden Schadensmeldung.
Das Bundesamt schaut eifrig zu
Eine Aufgabe des BASG im Bereich Medizinprodukte ist die Vigilanz,
schreibt das BASG zur Causa auf Semiosis-Anfrage. Der Ausdruck „Vigilanz“ kommt aus der Psychologie und bedeutet so viel wie „Aufmerksamkeit“ bei „eintöniger Reizfrequenz“. So gab es außer dem Hinweis auf der Homepage (unter dem sinnigen Menüpunkt „Marktbeobachtung“) keine weitere öffentliche Information. Was das Amt in der Antwort auf unsere Anfrage mit der staatlich verordneten Unparteilichkeit erklärt.
Philips ruft über fünf Millionen Geräte zurück
Mittlerweile hat der Konzern angekündigt, dass er weltweit mehr als fünf Millionen Geräte zurückrufen müsse. Ursprünglich ging man von nur vier Millionen Geräten aus. An den Aktienmärkten führe das natürlich zu Problemen. Die Aktie brach ein.
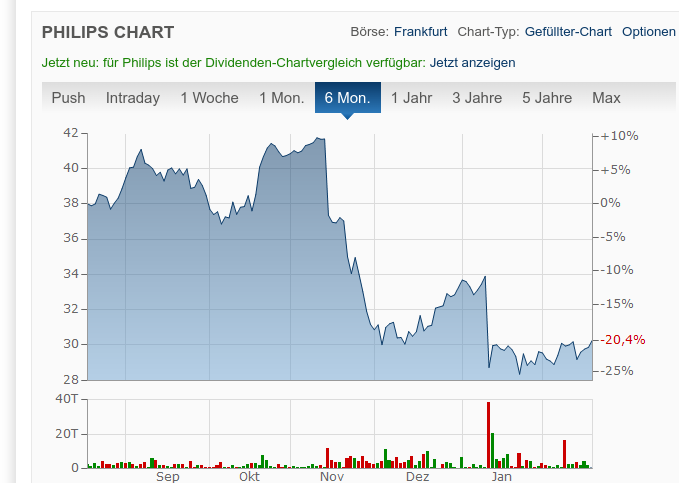
Dabei würden sich die Kosten der Rückrufaktion auf 720 Millionen Euro summieren, berichtet das Handelsblatt.
Klagen von Patienten sind dabei noch nicht eingerechnet.
Informationen zum Fall
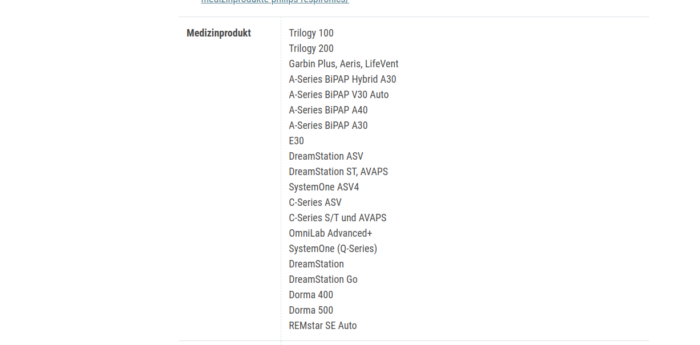
Betroffene Geräte (laut Angaben von Philips)





1 thought on “BASG: Das österreichische Nachtwächteramt”
Comments are closed.